Noch bestehen elektronische Geräte aus unbelebten Materialien. Eines Tages könnten jedoch „mikrobielle Cyborgs“, also stromerzeugende Kleinstlebewesen, Anwendung in Brennstoffzellen, Biosensoren oder Bioreaktoren finden.
Ein Bakterium, das dafür infrage kommt, ist Shewanella oneidensis. Es gehört zu den sogenannten exoelektrogenen Bakterien, die im Stoffwechselprozess Elektronen erzeugen und zur Außenseite der Zelle transportieren können.
Der Versuch, diese Elektrizität nutzbar zu machen, war jedoch immer durch eine eingeschränkte Interaktion der Organismen mit der Elektrode begrenzt. Im Unterschied zu herkömmlichen Batterien muss das Material bei dieser „Biobatterie“ nicht nur die Elektronen zu einer Elektrode leiten, sondern zugleich möglichst viele Bakterien optimal mit der Elektrode verbinden. Solche Materialien waren bislang aber entweder ineffizient oder es fehlte die Möglichkeit, den elektrischen Strom zu steuern.
Nährboden für stromerzeugende Bakterien
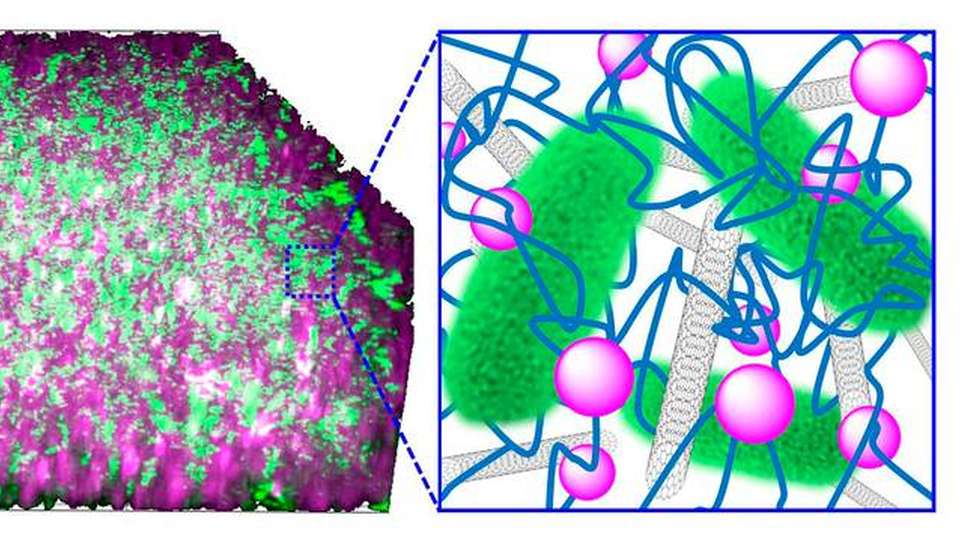
Dem Team um Professor Christof Niemeyer vom Karlsruher Institut für Technologie (KIT) gelang es nun, ein Nanokomposit-Material zu entwickeln, das das Wachstum von exoelektrogenen Bakterien unterstützt und zugleich den Strom kontrolliert leitet. „Wir haben dazu ein poröses Hydrogel hergestellt, das aus Kohlenstoff-Nanoröhrchen und Kieselsäure-Nanopartikeln besteht“, erklärt Niemeyer. „Diese sind durch DNA-Stränge miteinander verwoben.“
Dem Gerüst fügte die Arbeitsgruppe das Bakterium Shewanella oneidensis sowie ein flüssiges Nährmedium zu. Die Kombination aus verschiedenen Materialien und Mikroben funktionierte: „Die Kultivierung von Shewanella oneidensis in den leitfähigen Materialien zeigt, dass die exoelektrogenen Bakterien das Gerüst besiedeln, während andere Bakterien, wie zum Beispiel Escherichia coli, nur auf der Oberfläche der Matrix bleiben“, erläutert der Mikrobiologe Prof. Johannes Gescher.
Darüber hinaus konnte das Forschungsteam belegen, dass der Elektronenfluss zunahm, je mehr Bakterienzellen die leitfähige, synthetische Matrix besiedelten. Dieser biohybride Verbund blieb mehrere Tage lang stabil und zeigte elektrochemische Aktivität: ein Beleg, dass das Verbundmaterial die von den Bakterien produzierten Elektronen effizient zu einer Elektrode leiten kann.
Prozesssteuerung per Enzym
Neben der Leitfähigkeit benötigt ein solches System auch die Möglichkeit, den Prozess zu steuern. Auch dies gelang im Experiment: Um den Strom abzuschalten, fügten die Forschenden ein Enzym hinzu, das DNA-Stränge zerschneidet, wodurch das Verbundmaterial zerlegt wurde.
„Nach unserer Kenntnis ist es bisher das erste Mal, dass ein solch komplexes und funktionelles biohybrides Material beschrieben wurde“, berichtet Niemeyer. Insgesamt deuten die Ergebnisse laut ihm darauf hin, „dass mögliche Anwendungen solcher Materialien sogar über mikrobielle Biosensoren, Bioreaktoren und Brennstoffzellensysteme hinausgehen könnten.“