„Wasserstoff ist ein sauberer Brennstoff für die Energieerzeugung“, konstatiert Mitverfasser Johann Heider, der Mikrobiologie an der Philipps-Universität Marburg lehrt. „Außerdem taugt er als billiges Reduktionsmittel für die Herstellung nützlicher Verbindungen aus Biomasse.“
Hydrogenase-Enzyme erfüllen dabei unterschiedliche Funktionen. Einerseits entziehen sie dem Wasserstoff Elektronen, die sie dann für biologische Reaktionen einsetzen. Andererseits erzeugen Hydrogenasen Wasserstoff aus Protonen und geeigneten Elektronenüberträgern.
„Die bisher bekannten Hydrogenasen enthalten Nickel- und Eisen-Atome und sind schwer handhabbar“, erläutert Heider. „Denn meistens sind sie sehr empfindlich gegen Sauerstoff oder Kohlenmonoxid, die in technischen Anwendungen oft zum Wasserstoff beigemischt sind.“
Aldehyd-Oxidoreduktase
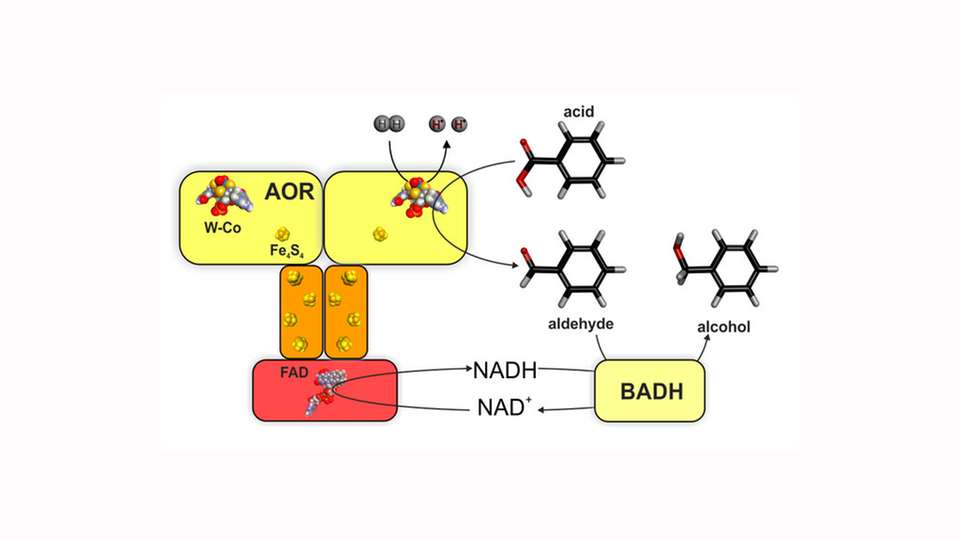
Heiders Arbeitsgruppe an der Philipps-Universität tat sich mit Professor Dr. Maciej Szaleniec vom Jerzy-Haber-Institut in Krakau zusammen, um das wolframhaltige Enzym Aldehyd-Oxidoreduktase (AOR) zu erforschen, das in Bakterien vorkommt. Das Team wies erstmals nach, dass auch dieses Enzym in der Lage ist, Wasserstoff als Reduktionsmittel für biochemische Reaktionen zu verwenden: „Wir geben Beispiele für die Kopplung von AOR an industriell wichtige Substanzen, die in der Feinchemie und der pharmazeutischen Industrie eingesetzt werden“, sagt Heider.
Eine andere Funktion des Enzyms besteht in der Umwandlung von organischen Säuren zu Aldehyden. „Dies kann genutzt werden, um Abfallstoffe aus Holz mittels ‘grüner‘ Biochemie zu wertvollen Chemikalien zu veredeln, die zum Beispiel als Treibstoffe dienen können“, legt der Marburger Hochschullehrer dar. Aber das ist noch nicht alles, wie er weiter ausführt: AOR ist außerdem viel unempfindlicher gegen Sauerstoff und Kohlenmonoxid als die bisher bekannten Hydrogenasen.












.jpg)
